FAG Originalartikkel
Venøs blodprøvetaking i Norge – en observasjonsstudie
Hovedbudskap
- I 2013 ble det gjennomført en europeisk observasjonsstudie i 12 land for å vurdere etterlevelse av CLSI sine retningslinjer for venøs blodprøvetaking.
- Den norske delen av studien omfattet bioingeniører, helsesekretærer og sykepleiere fra utvalgte avdelinger knyttet til tre sykehus.
- Observasjonene og risikoanalyse viste at grad av etterlevelse er lav i Norge, og at de mest kritiske områdene er knyttet til pasientidentifikasjon og merking av prøveglass.
Venøs blodprøvetaking i Norge – en observasjonsstudie.pdf(361 KB)
Innledning
Den preanalytiske fasen er i dag kjent som den viktigste bidragsyteren til diagnostiske feil innen laboratoriemedisin (1). Venøs blodprøvetaking, som er en viktig del av den preanalytiske fasen, er den mest vanlige invasive prosedyren som utføres i helsevesenet (2,3). Blodprøvetaking er en kompleks prosedyre som krever både kunnskap og kompetanse. Den inkluderer mange trinn og feil håndtering kan få alvorlige konsekvenser som kan påvirke pasientens sikkerhet. Dårlige rutiner og mangel på standardisering kan føre til forsinkelser eller feil i analyseresultatet, og i mange tilfeller må prøven også tas på nytt. Det blir tatt blodprøver i mange ulike situasjoner, ofte utenfor laboratoriet, og mange ulike helsepersonellgrupper er involvert (4). Feil som oppstår under blodprøvetaking kan derfor være vanskelig å adressere og korrigere.
Standardiserte prøvetakingsrutiner er vesentlig for et riktig analyseresultat (5, 6). Det finnes flere retningslinjer som beskriver hvordan korrekt blodprøvetaking skal utføres (7,8), men det er lite kunnskap om hvordan blodprøvetakingen utføres i praksis. I de skandinaviske landene er det kun Sverige som har nasjonale retningslinjer (9). I Norge er det nylig publisert en fagprosedyre for venøs blodprøvetaking basert på kunnskapsbaserte retningslinjer (10). For å standardisere medisinsk behandling og ivareta pasientsikkerheten er det viktig at retningslinjer/prosedyrer etterleves (11, 12). Spørreundersøkelser (med selvrapporterte data) har nylig vist at helsepersonell på sykehus og i primærhelsetjenesten (PHT) i varierende grad etterlever retningslinjer for venøs blodprøvetaking (13, 14, 15, 16).
European Federation of Clinical Chemistry and Laboratory Medicine (EFLM) opprettet en arbeidsgruppe for den preanalytiske fase i 2010 (EFLM WG-PRE). I løpet av 2013 utførte arbeidsgruppen en observasjonsstudie for å vurdere etterlevelse av Clinical and Laboratory Standards Institute (CLSI) sine retningslinjer for venøs prøvetaking (CLSI H3-A6) i Europa og for å identifisere de mest kritiske trinn i prøvetakingsprosessen (17). Tolv europeiske land deltok og observasjoner fra ett sykehus fra hvert land ble inkludert i studien. I Norge ble det gjennomført observasjoner ved totalt tre ulike sykehus; Diakonhjemmet Sykehus, Haukeland universitetssjukehus og St. Olavs Hospital. I denne artikkelen er alle de norske resultatene inkludert. Hensikten har vært å få mer kunnskap om hvordan blodprøvetaking utføres i Norge, og dokumentere hvem som tar blodprøver og i hvor stor grad CLSI retningslinjene blir fulgt her i landet. Samtidig ville vi utføre en risikoanalyse for å identifisere de mest kritiske trinn i prøvetakingsprosessen.
Materiale og Metode
Studiedesign
Observasjonsstudiene ble gjennomført fra mai til september 2013. En sjekkliste med 29 spørsmål ble benyttet der de fleste spørsmålene kunne besvares med ja eller nei. Sjekklisten var basert på CLSI H3-A6 retningslinjer for venøs prøvetaking (7), og utarbeidet av EFLM WG-PRE (17). På tre ulike avdelinger ved hvert sykehus; akuttmottak, klinisk avdeling og prøvetakingspoliklinikk, ble tre prøvetakere observert av en bioingeniør mens de utførte tre venøse blodprøvetakinger hver. Bioingeniører med ansvar for blodprøvetaking ble valgt som observatører. Totalt ble det gjennomført 3 x 3 = 9 observasjoner ved hver avdeling og totalt 3 x 9 = 27 observasjoner ved hvert sykehus. I tillegg ble tre prøvetakere som utførte tre venøse blodprøvetakinger hver på legekontor i nærområdet til hvert av de tre deltakende sykehus, observert av fagkonsulenter fra Norsk kvalitetsforbedring av laboratorievirksomhet utenfor sykehus (Noklus). Totalt ble det gjennomført 108 observasjoner av venøs blodprøvetaking i studien.
Dataanalyse
Svaralternativene ble kategorisert som «ja», «nei» eller «ikke aktuell» (17). Positivt svaralternativ (ja) vil i de fleste tilfeller bety at prøvetakingen som ble observert, var i samsvar med CLSI sine retningslinjer. På spørsmålet «Når ble prøverørene merket?» var det ønskede svaret etter prøvetaking. Spørsmålet «Ble prøverørene merket ved siden av pasienten?» er kun analysert der prøvene ble merket etter prøvetaking. Forskjell mellom grupper ble analysert med Chi-square test. Signifikansnivå ble satt til 0,001 på grunn av multiple sammenligninger (18).
Risikoanalyse
For å identifisere de mest kritiske trinn i prøvetakingsprosessen ble det utført en risikoanalyse tilsvarende det som ble gjort i den europeiske studien (17). Sannsynlighet for feil og alvorlighetsgraden av feil som oppstår under blodprøvetaking, ble vurdert ved hjelp av en semi-kvantitativ metode ved bruk av to skjemaer (Tabell 1 og 2) (19). Sannsynlighet for feil ble vurdert utfra tabell 1 for hvert av de 29 spørsmålene i sjekklisten, basert på den gjennomsnittlige feilfrekvens observert under studien, fra sjelden (01) til hyppig (06). En gjennomsnittlig feilfrekvens på 70 % ga for eksempel score på 05. Alvorlighetsgraden av feil ble vurdert fra ubetydelig (S1) til livstruende (S5), basert på tabell 2. Alle medlemmene i den europeiske arbeidsgruppen (EFLM WG-PRE) vurderte alvorlighetsgrad av feil for hvert av de 29 spørsmålene i sjekklisten individuelt, og median ble brukt til videre analyse (17).
Tabell 1: Scoringssystem for sannsynlighet for feil.
| Forekomst | Forkortelse | Definisjon | Sannsynlighet for feil |
| Sjelden | O1 | Skade skjer sannsynligvis ikke | < 1 % |
| Usannsynlig | O2 | Skade skjer veldig sjelden | 1 - 10 % |
| Mindre sannsynlig | O3 | Skade er ikke sterkt sannsynlig | 10 - 20 % |
| Sporadisk | O4 | Skade skjer sporadisk | 20 - 50 % |
| Sannsynlig | O5 | Skade er nesten sikker | 50 - 75 % |
| Hyppig | O6 | Skade er sikker | > 75 % |
Tabell 2: Scoringssystem for alvorlighetsgrad av feil
| Vurdering | Forkortelse | Definisjon |
| Ubetydelig | S1 | Ingen virkning |
| Begrenset | S2 | Unødvendig ekstra prøvetaking |
| Moderat | S3 | Forsinket diagnose |
| Alvorlig | S4 | Mangelfull behandling på grunn av unøyaktige laboratorieresultater |
| Livstruende | S5 | Feil transfusjon |
Resultater
Tre norske sykehus deltok i undersøkelsen; Diakonhjemmet Sykehus i Oslo, Haukeland universitetssjukehus i Bergen og St. Olavs Hospital i Trondheim. Det ble utført like mange observasjoner på hvert sykehus og tilknyttede legekontor. Totalt ble det gjennomført 108 observasjoner fordelt på fire avdelinger; akuttmottak (n=27), kliniske avdelinger (n=27), laboratoriets poliklinikk (n=27) og legekontor lokalisert nær hvert sykehus (n=27).
Venøs blodprøvetaking ble utført av tre typer helsepersonell; bioingeniører, helsesekretærer og sykepleiere, der bioingeniørene utgjorde den største gruppen. Tabell 3 gir en oversikt over hvor mange blodprøver de tre helsepersonellgruppene tok ved hver av de ulike avdelingene. Bioingeniører tok blodprøver på alle avdelinger på sykehus, mens sykepleiere hovedsakelig tok blodprøver i akuttmottak. Helsesekretærer var den eneste helsepersonellgruppen som tok blodprøver på legekontorene.
Tabell 3: Fordeling av observerte prøvetakinger etter helsepersonellgruppe og avdeling
| Helsepersonellgruppe | Akuttmottak | Kliniske avdelinger | Laboratoriets poliklinikk | Legekontor |
| Bioingeniør (n=45) | 9 | 18 | 18 | 0 |
| Helsesekretær (n=36) | 0 | 0 | 9 | 27 |
| Sykepleier (n=27) | 18 | 9 | 0 | 0 |
| Totalt (n=108) | 27 | 27 | 27 | 27 |
Resultater fra 108 observerte venøse blodprøvetakinger er oppsummert i tabell 4. Feilfrekvens (%) og vurdering av sannsynlighet og alvorlighetsgrad av feil, samt p-verdi for beregnede forskjeller mellom ulike avdelinger og ulike helsepersonellgrupper, er tatt med i tabellen.
Gjennomsnittlig feilfrekvens var 26 %. Prøvetakere i Norge følger ikke CLSIs retningslinjer når det gjelder flere trinn i prøvetakingsprosedyren. Dette gjelder spesielt spørsmål 3, 11, 12, 24 og 28 med henholdsvis 100, 89, 70, 97 og 76 % feilfrekvens. For spørsmål 4, 5, 7, 8, 12, 19 og 29, ble det funnet signifikante forskjeller mellom både avdeling (hvor prøven ble tatt) og helsepersonellgruppe (hvem som tok prøven), mens for spørsmål 6, 15, 16, 20, 22, 26 og 28 ble det funnet signifikante forskjeller mellom enten avdeling eller helsepersonellgruppe. På spørsmål 7 og 8 svarte imidlertid omtrent en tredel at spørsmålene ikke var aktuelle, og tilsvarende på spørsmål 13 og 14 der omtrent halvparten svarte dette.
Spørsmålene 2, 3, 7, 17 og 25 er knyttet til den overordnede organisering av prøvetakingsrutinene og gjenspeiler i mindre grad hvordan den individuelle prøvetaker forholder seg til prosedyren. Spørsmålet «Har prøvetaker kontrollert prøvetakingsutstyrets holdbarhet?» dekker en oppgave som oftest ivaretas av laboratoriet og ikke av den enkelte. Tilsvarende er spørsmål 2 (om rekvisisjon), 7 (om prøvetakingsstol), 17 (om lukket prøvetakingssystem) og 25 (når prøvene ble merket) lite relevant for hvordan den enkelte prøvetaker forholder seg til prosedyren. Her er det laboratorienes eller legekontorenes overordnede retningslinjer som avgjør.
Resultatene fra risikoanalysen er oppsummert i tabell 5, der risikoen er fordelt i grønn, gul eller rød sone. Grønn sone indikerer at arbeidsprosessen ikke krever risikoreduserende tiltak. Gul sone angir at arbeidsprosessen har så lav risiko som praktisk mulig, men her bør man prøve å redusere risikoen. Arbeidsprosesser som er i rød sone krever at det øyeblikkelig iverksettes tiltak for å redusere alvorlige eller livstruende situasjoner. Spørsmål 3, 4, 11, 12, 24, 25, og 26 er i rød sone. Spørsmål 4, 25 og 26 er knyttet til identifisering av pasient og merking av prøver. Spørsmål 3 er knyttet til å kontrollere holdbarhet på prøverørene. Spørsmål 11 og 12 er knyttet til hanskebruk og desinfisering av stikkstedet før prøvetaking, og spørsmål 24 er relatert til om prøvetaker advarer pasienten mot å bøye armen etter prøvetaking.
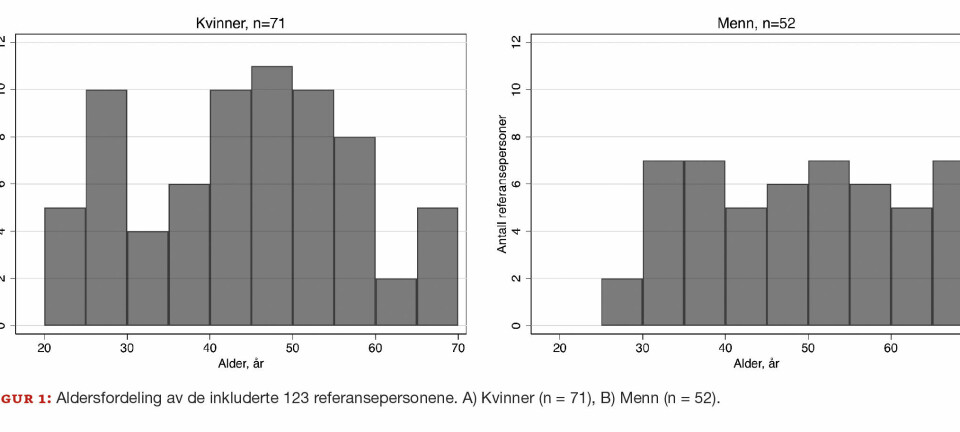
For tre av spørsmålene i rød sone; spørsmål 4, 12 og 26, ble det påvist signifikant forskjell i feilfrekvens avhengig av hvor prøven ble tatt og/eller hvem som tok prøven. For spørsmålet «Har prøvetaker identifisert pasienten iht. CLSI eller lokale retningslinjer?» ble det påvist forskjell i feilfrekvens både mellom ulike avdelinger og mellom ulike helsepersonellgrupper. Halvparten av helsesekretærene (51 %) identifiserte ikke pasienten i henhold til CLSI eller lokale retningslinjer (figur 1).
For spørsmålet «Rengjorde prøvetaker punksjonsstedet?» ble det også påvist forskjell i feilfrekvens både mellom ulike avdelinger og mellom ulike helsepersonellgrupper. Helsesekretærer var mest tilbøyelig til ikke å rengjøre punksjonsstedet før blodprøvetaking mens sykepleiere rengjorde punksjonsstedet oftest før de tok blodprøve. På legekontor var det ingen som rengjorde punksjonsstedet før blodprøvetaking (figur 2).
For spørsmålet «Ble prøverørene merket ved siden av pasienten?» ble det påvist signifikant forskjell i feilfrekvens mellom ulike avdelinger. På de kliniske avdelingene (58 %) og på legekontor (36 %) var det flest som ikke merket prøverørene ved siden av pasienten (figur 3). Det var også forskjell i feilfrekvens mellom de ulike helsepersonellgruppene, og sykepleiere merket prøverørene oftest i nærvær av pasienten. Denne forskjellen var imidlertid ikke signifikant og er derfor ikke inkludert i figuren.
Diskusjon
Hensikten med denne studien var å undersøke hvordan blodprøvetaking utføres i Norge, hvem som tar blodprøver og i hvor stor grad CLSI retningslinjene blir etterlevd. Vi ønsket også å identifisere de mest kritiske trinn i prøvetakingsprosessen. Hovedfunnet er at etterlevelse av CLSI H3-A6 retningslinjer for venøs blodprøvetaking er lav i Norge. Alle sykehusene hadde lokale retningslinjer for venøs blodprøvetaking, som i hovedsak var basert på retningslinjene fra CLSI, men med noen avvik. Blant de tre helsepersonellgruppene som tar blodprøver var det flest bioingeniører, dernest helsesekretærer og noe færre sykepleiere. På legekontor var det kun helsesekretærer som tok blodprøver. Pasientidentifikasjon og merking av prøverør ble vurdert som de mest kritiske trinn som krever umiddelbar handling, noe som er i samsvar med funn fra den europeiske studien utført av Simundic og medarbeidere (17). I tillegg viste resultatene at det i Norge ikke er vanlig å bruke hansker eller å desinfisere punksjonsstedet ved venøs blodprøvetaking.
Generelle årsaker til at retningslinjer ikke følges kan være manglende teoretiske kunnskaper eller at en ikke er kjent med retningslinjene. Samtidig kan holdninger til retningslinjer, arbeidspress og tidsklemme nevnes som mulige årsaker (20). I denne studien har vi forsøkt å dokumentere avvik fra retningslinjene, uten å gjøre videre undersøkelser på årsakene til at de ikke følges.
I følge risikoanalysen i vår studie plasserte resultatene for spørsmål 3, 4, 11, 12, 24, 25 og 26 seg i den kritiske røde sone som hadde den høyeste kombinasjon av sannsynlighet for feil og alvorlighetsgrad (tabell 5). Spørsmål 3 og 25 er relatert til overordnet praksis ved avdelingen og ble derfor ikke analysert nærmere. De aller fleste i Norge (99 %) fulgte imidlertid CLSI’s anbefaling om å merke prøverørene etter at blodprøven var tatt. Grunnen til at denne feilen havnet i rød sone til tross for lav feilfrekvens, er at den er vurdert som mulig livstruende (Tabell 2).
Feil identifisering av pasient i forbindelse med blodprøvetaking kan få alvorlige konsekvenser (21, 22). Tabell 4 viser at 23 % av prøvetakerne ikke identifiserer pasienten korrekt i henhold til CLSI retningslinjene. Både helsesekretærer og sykepleiere unnlater å spørre om navn og fødselsnummer/dato (figur 1). Resultatene viser også at mangelfull/ukorrekt identifisering av pasienten skjer oftest på legekontor. Svenske undersøkelser viser tilsvarende funn i PHT (14,15, 23). En av grunnene til mangelfulle rutiner er at prøvetaker mener at de kjenner pasientene (15, 24). I 2014 og 2015 har medisinske laboratorier i Norge registrert preanalytiske feil på tilsendte prøver fra PHT, deriblant prøver med feil pasientidentifikasjon. Ifølge anbefalt kravspesifikasjon fra International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) er en feilfrekvens > 0,6 % uakseptabelt (25). De norske laboratoriene registrerte i 2014 en gjennomsnittlig feilfrekvens med hensyn til korrekt pasientidentifikasjon på tilsendte prøver fra PHT på 0,6 %, altså helt på grensen til uakseptabel (26). De senere år har det vært mye fokus på preanalytiske feil, og både sykehuslaboratoriene og Noklus har arbeidet aktivt for bedre pasientidentifikasjon i PHT. I 2015 var den gjennomsnittlige feilfrekvensen redusert til 0,4 % (upubliserte resultater fra Nasjonal dugnad for registrering av preanalytiske feil fra PHT, 2015). I de preanalytiske eksterne kvalitetsvurderinger (EKV) sendt fra Noklus til PHT, ser man at andel feil med hensyn til korrekt pasientidentifikasjon er redusert i perioden 2013 til 2015 (upubliserte data). I tillegg økte andel laboratorier med elektronisk rekvirering fra 2014 til 2015, noe som også kan ha bidratt til reduksjon av feil pasientidentifikasjon (upubliserte resultater fra Nasjonal dugnad for registrering av preanalytiske feil fra PHT, 2015). Elektronisk rekvirering kan redusere feil knyttet til pasientidentifikasjon og rekvirering, men kan fortsatt ikke eliminere feil knyttet til identifikasjonspraksis der en forbytter pasienter eller prøverør.
Feilmerking er vanlig (27) og kan utgjøre 50 % av alle identifikasjonsfeil (28). Figur 3 viser at personalet som tar blodprøver har ulik praksis når det gjelder å merke prøverørene umiddelbart ved siden av pasienten. 27 % av prøvetakerne merket ikke prøverørene ved siden av pasienten. Personalet som tar blodprøver på kliniske avdelinger er minst tilbøyelig til å merke prøverøret i nærheten av pasienten. Wallin rapporterer også at personalet merker rørene ved en senere anledning (29). Retningslinjene fra CLSI (7) og WHO (22) er svært tydelig på at prøverørene skal merkes umiddelbart i nærvær av pasienten. Det samme gjelder veileder for transfusjonstjenesten (30). Praksis med hensyn til om merking av prøverørene skjer i nærvær av pasienten viser ingen forskjell mellom profesjonene, derimot har det betydning hvor prøven blir tatt. Dette kan tyde på at praktiske forhold på stedet hvor prøven blir tatt kan påvirke når prøverørene merkes. Prøvetakingen gjennomføres både i optimale prøvetakingsrom og i situasjoner som er langt fra ideelle, for eksempel i isolater, der rørene blir merket utenfor rommet. Sedvane kan også være årsak til at en ikke følger retningslinjene. At prøverør merkes i nærvær av pasienten er en viktig sikkerhetsbarriere for å hindre at pasientenes identitet forbyttes.
Som det fremgår av tabell 4 er det 89 % av prøvetakere som ikke følger CLSI sine retningslinjer i henhold til bruk av hansker mens 70 % ikke følger retningslinjene når det gjelder desinfeksjon av huden før prøvetaking. Venøs blodprøvetaking medfører vanligvis ikke at en kommer i kontakt med blod eller kroppsvæsker eller utsettes for blodsøl. Norske helsemyndigheter anbefaler at en skal benytte hansker til konkrete arbeidsoppgaver der det er fare for overføring av smittestoffer (31). Hansker bør benyttes ved venøs blodprøvetaking (10). Dette gjelder spesielt dersom det er bekreftet blodsmitte, fare for blodsøl, for eksempel ved prøvetaking på urolige pasienter, eller dersom prøvetaker ikke har hel hud (3). Desinfeksjon av huden før venøs prøvetaking har tradisjonelt ikke vært anbefalt fra Folkehelseinstituttet (FHI). Først i 2009 anbefalte norske myndigheter å desinfisere før prøvetaking som et «føre var-prinsipp» (32). Figur 3 viser at sykepleiere er mest opptatt av å desinfiserer huden før prøvetaking, sannsynligvis fordi sykepleiefaglige rutiner anbefaler å desinfisere før injeksjoner og andre invasive prosedyrer. Nye retningslinjer for venøs blodprøvetaking anbefaler i dag å desinfisere/vaske huden selv om den faglige argumentasjonen er svak (10).
Tilsvarende viser resultatene at det er et fåtall av prøvetakere som advarer pasientene mot å bøye armen etter prøvetaking. I følge CLSI sin retningslinje skal en pasient ikke få lov å bøye armen opp som en erstatning for komprimering av stikkstedet, da denne teknikken ikke er tilstrekkelig til å hindre dannelse hematom (7). Å advare pasienten mot å bøye armen for å hindre blødning og dannelse av hematom, har etter vår vurdering en svært svak faglig begrunnelse. En dansk studie har vist at det ikke er noen forskjell med hensyn til blødning om armen er bøyd eller ikke (33). Verken i Danmark, Sverige eller Norge er dette punktet tatt med i de retningslinjer/prosedyrer som benyttes for venøs blodprøvetaking. Det viktigste tiltaket for å redusere blødning er å komprimere stikkstedet. Erfaringsmessig er det relativt lite hudblødninger i forbindelse med venøs blodprøvetaking. Vi er uenig i at dette punktet i CLSIs retningslinjer er av vesentlig betydning. Dersom feilene knyttet til kontroll av prøvetakingsutstyrets holdbarhet og advarsel mot å bøye armen ekskluderes, vil den gjennomsnittlige feilprosenten i denne studien reduseres fra 26 til 19 %.
Prøvetakingsrutiner i Norge avviker fra CLSI sine retningslinjer for spørsmål 11, 12, 24 og 28. Når det gjelder hanskebruk og desinfeksjon av punksjonsstedet skyldes det sannsynligvis nasjonale anbefalinger og lokal praksis/retningslinjer. Det å advare pasienten mot å bøye armen etter prøvetaking er ikke vanlig praksis i Norge der vi legger større vekt på å komprimere stikkstedet. Videre viser resultatene at det er få prøvetakere som undersøker for potensielle komplikasjoner ved venepunksjon, noe som kan gjenspeile at prøvetakingen var problemfri, og at det derfor ikke har vært behov for dette.
Få land i Europa har nasjonale retningslinjer (4). Norge har ikke nasjonale retningslinjer, men det er derimot nylig publisert fagprosedyrer for venøs og kapillær blodprøvetaking basert på kunnskapsbaserte retningslinjer (10). Alle de norske sykehusene som deltok i denne studien oppga at de har lokale retningslinjer delvis basert på CLSI sine retningslinjer, men at retningslinjene er tilpasset lokale eller nasjonale forhold. I PHT benyttes enten sykehusenes retningslinjer eller retningslinjer fra Noklus. Den preanalytiske arbeidsgruppen fra EFLM (WG-PRE) jobber med en harmonisering av europeiske retningslinjer for venøs blodprøvetaking for å gjøre dem mer fokuserte, enklere, mer brukervennlig og bedre tilpasset praktisk bruk. Det vil imidlertid bli presisert at dersom det er diskrepans sammenlignet med nasjonale retningslinjer, er de nasjonale overstyrende.
Konklusjon
Observasjonsstudier av venøs blodprøvetaking ved bruk av sjekkliste og risikoanalyse er en effektiv metode for å vurdere kritiske trinn i prøvetakingsprosessen. Vår studie viser at grad av etterlevelse av CLSI sine retningslinjer for venøs blodprøvetaking er lav i Norge, spesielt når det gjelder pasientidentifikasjon og merking av prøverør, samt bruk av hansker og desinfisering av punksjonsstedet før prøvetaking. Korrekt identifisering av pasienten er helt avgjørende for å ivareta pasientsikkerheten. De senere år har det vært satt inn ressurser for å eliminere slike feil og vi ser en positiv utvikling. Vi anbefaler kontinuerlig overvåkning av preanalytiske feil, fortrinnsvis ved gjentatt observasjon av prøvetakingspraksis.
Takk
Takk til bioingeniørene på de tre sykehusene som hjalp til med datainnsamlingen. Takk til alle prøvetakere som deltok i observasjonsstudien.
Spesiell takk til May-Britt Solem på Diakonhjemmet, og Kristine Bodal Solem og Hilde Hegseth på St. Olavs Hospital som organiserte innsamling av data på de respektive sykehusene.